La hepatitis B es una infección viral de larga duración del hígado. Los tratamientos actuales pueden suprimir el virus de la hepatitis B pero no ofrecen la oportunidad de curación, por lo que se requieren nuevos enfoques de tratamiento.
En este documento, mostramos que la combinación del nuevo inhibidor central vebicorvir con un antiviral existente (entecavir) en pacientes sin tratamiento previo con infección crónica por el virus de la hepatitis B demostró una mayor actividad antiviral que el entecavir solo. Además, vebicorvir fue seguro y bien tolerado. Por lo tanto, se justifican más estudios que evalúen su papel potencial en el tratamiento de la hepatitis B crónica.
Puntos destacados:
- La supresión completa de la replicación del VHB es esencial para los regímenes de tratamiento finitos.
- Vebicorvir (VBR) es un inhibidor de la proteína central del VHB desarrollado para tratar el VHB crónico.
- VBR interfiere con 2 pasos adicionales en la replicación del VHB y, por lo tanto, complementa a NrtI.
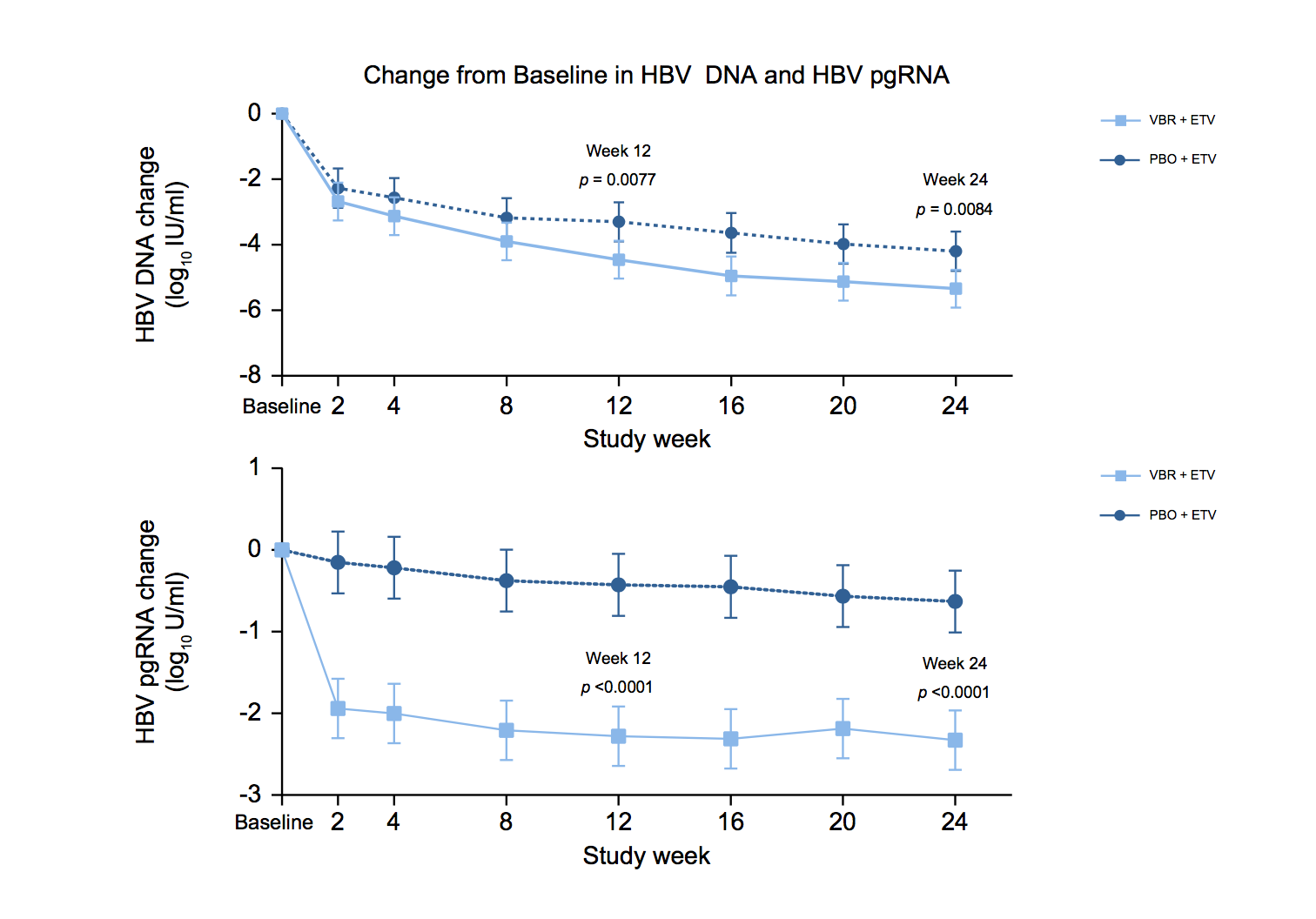
- VBR + ETV (entecavir) condujo a una reducción significativamente más profunda en el ADN del VHB y el ARN pregenómico que ETV solo.
- VBR+ETV se asoció con seguridad y tolerabilidad favorables durante 24 semanas de tratamiento.
Introducción
En todo el mundo, se estima que más de 250 millones de personas tienen una infección crónica por el VHB, y unas 800.000 personas mueren cada año de cirrosis o carcinoma hepatocelular relacionado con el VHB. Los inhibidores de la transcriptasa inversa nucleósidos (NrtI) se administran por vía oral y pueden reducir la producción de viriones a través de varios mecanismos, incluido el bloqueo de la transcripción inversa del ARN pregenómico (pg) al ADN del VHB, la prevención de la elongación del ADN y la inhibición del cebado de la proteína del VHB. En general, son bien tolerados y los NrtI de segunda generación (es decir, entecavir [ETV] y tenofovir) tienen altas barreras a la resistencia. Sin embargo, no suprimen completamente la replicación viral, con estudios que demuestran que aproximadamente el 40% de los pacientes con HBeAg positivo y el 10% de los pacientes con HBeAg negativo continúan teniendo niveles detectables de ADN del VHB 1 año después del inicio del tratamiento. La viremia residual permanece debido a la incapacidad de los NrtI para suprimir por completo la replicación del VHB y eliminar el VHB cerrado covalentemente. ADN circular (ccc), la plantilla principal para la replicación del VHB. Por lo tanto, el tratamiento a largo plazo con NrtI es necesario para la mayoría de los pacientes.
Los inhibidores del núcleo son una nueva clase de moléculas pequeñas que se están evaluando para el tratamiento del VHB crónico (cHBV). Los inhibidores del núcleo interfieren con múltiples aspectos del ciclo de replicación del VHB, incluido el proceso de ensamblaje de la cápside, la encapsidación del pgRNA y la formación de nuevo ADN circular covalentemente cerrado (cccDNA). Los inhibidores del núcleo han demostrado actividad contra los genotipos conocidos del VHB, y la prevalencia inicial de variantes resistentes es baja. La seguridad ha sido una preocupación para algunos inhibidores del núcleo experimentales, que se han asociado con eventos adversos gastrointestinales (AA) y elevaciones de alanina aminotransferasa (ALT).
Vebicorvir (VBR) es un inhibidor central pangenotípico, potente, selectivo y administrado por vía oral que induce un ensamblaje de proteína central alterado y no funcional. En un estudio de fase Ib aleatorizado, controlado con placebo en pacientes con VHBc , VBR en dosis de hasta 300 mg/día durante 28 días fue bien tolerado, sin patrón de AA emergentes del tratamiento (TEAE). VBR 100, 200 y 300 mg administrados una vez al día demostraron disminuciones dependientes de la dosis en el ADN del VHB y el ARN del VHB en suero, de acuerdo con su mecanismo de acción.
Al interferir con 2 pasos adicionales en la replicación del VHB, la adición de VBR a la terapia con NrtI tiene el potencial de mejorar la actividad antiviral en pacientes con VHBc mientras mantiene una alta barrera a la resistencia. El objetivo de este estudio de fase II fue evaluar la seguridad y eficacia de VBR más NrtI en pacientes sin tratamiento previo con cHBV HBeAg positivo y para probar la hipótesis de que la adición de VBR conduciría a una mayor supresión de la viremia del VHB.
Debate
Los inhibidores centrales son prometedores como un tratamiento novedoso en cHBV, ya que el ensamblaje y desensamblaje de la cápside son pasos críticos en la producción de virus, así como en la generación de cccDNA. En este ensayo de fase II aleatorizado y controlado con placebo, probamos la hipótesis de que el bloqueo de pasos adicionales en el ciclo de replicación del VHB mediante la adición de VBR a ETV conduciría a una mayor respuesta virológica que entecavir solo en pacientes sin tratamiento previo con VHBc positivo para HBeAg. Se cumplieron los criterios de valoración coprimarios, con VBR+ETV dando como resultado reducciones significativamente mayores en el ADN del VHB desde el inicio en las semanas 12 y 24 en comparación con PBO+ETV.
Los pacientes que recibieron VBR+ETV demostraron niveles más rápidos y profundos de supresión del ADN del VHB que los que recibieron PBO+ETV. En la semana 24, más pacientes que recibieron VBR+ETV lograron ADN del VHB indetectable que los que recibieron PBO+ETV. Los pacientes que recibieron VBR+ETV también demostraron disminuciones significativamente mayores en pgRNA. La contribución de VBR a ETV se observó ya en la semana 2, con disminuciones en el ADN del VHB y pgRNA en todas las visitas posteriores hasta la semana 24. La única fuente de pgRNA es cccDNA y, en consecuencia, este marcador representa la medida más directa de cccDNA actividad transcripcional.
Las disminuciones en pgRNA de HBV observadas con VBR parecen ser bifásicas. Se ha observado un perfil similar con otros inhibidores centrales en desarrollo. Parece haber una reducción inicial aproximada de 2 log10 en el pgRNA del VHB, que se cree que representa la formación de cápsides vacíos que no contienen pgRNA. Se considera que la disminución de la primera fase está relacionada con el efecto farmacodinámico del inhibidor central y por lo tanto, se considera basado en mecanismos. Se postula que la segunda y más superficial disminución de la fase representa una disminución de la actividad transcripcional del cccDNA.
La mayoría de los pacientes a los que se les administró VBR+ETV experimentaron una disminución numérica en la ALT desde el inicio en la semana 24. Además, el porcentaje de pacientes con VBR+ETV que tenían ALT <−LSN se duplicó durante el transcurso del tratamiento, mientras que este porcentaje disminuyó en PBO+ETV. pacientes durante el estudio. Las reducciones medias de los antígenos del VHB fueron similares entre los tratamientos y, en algunos momentos, fueron numéricamente mayores en los pacientes que recibieron VBR+ETV frente a PBO+ETV. La profundidad de la supresión viral y el impacto sobre los antígenos pueden aumentar aún más con un tratamiento a más largo plazo.
Los hallazgos de seguridad y eficacia en el estudio son consistentes con los del estudio de fase Ib. En el estudio actual, ningún patrón de TEAE se asoció con VBR 300 mg, todos los EA fueron de intensidad leve o moderada y no hubo muertes ni lesiones graves. Los TEAE más comunes en cualquiera de los grupos de tratamiento fueron aumento de ALT, dolor de cabeza y prurito, sin que ocurriera ninguno en más de 2 pacientes en ninguno de los grupos. Todos los TEAE y las anomalías de laboratorio emergentes del tratamiento fueron de grado 1 o 2. Ningún paciente interrumpió el estudio debido a un TEAE. Es importante destacar que no se produjo ningún patrón de hepatotoxicidad con VBR+ETV.
Entre los pacientes que tenían niveles normales de ALT al inicio, las elevaciones de ALT fueron de grado 1 o 2, similares entre los grupos de tratamiento y consistentes con la historia natural de los pacientes con cHBV con replicación viral activa. Esto contrasta con las elevaciones de ALT de Grado 3 o 4 notificadas con algunos otros inhibidores centrales. A los pacientes de un estudio complementario que examinó a pacientes con VHB virológicamente suprimido que recibían NrtI también se les administró VBR (NCT03576066). Con la excepción del exantema, cuya incidencia fue mayor en los pacientes con supresión virológica que recibieron VBR+NrtI (12 eventos en total) en comparación con los eventos que no se informaron en el estudio actual, los hallazgos de seguridad y tolerabilidad fueron similares en los pacientes que recibieron VBR en ambos estudios.
La resistencia a los fármacos antivirales frente a los NrtI se debe a mutaciones en el gen de la polimerasa del VHB. A medida que se desarrollan agentes con otros mecanismos de acción, pueden surgir mutaciones adaptativas en otras secuencias de genes. Los virus que muestran sustituciones de aminoácidos pueden resultar en el fracaso del tratamiento y una susceptibilidad reducida al fármaco que se está utilizando, un reflejo de la resistencia antiviral. nivel de ADN, niveles séricos altos de ALT y supresión viral inadecuada con la terapia. Debido a que los inhibidores centrales y los NrtI tienen mecanismos de acción distintos, también se espera que la resistencia a esta combinación de tratamiento sea muy baja. No hubo casos del avance de la resistencia en pacientes VBR+ETV que cumplían con el tratamiento asignado.
Los 2 casos de rebote del ADN del VHB observados en el estudio (1 en cada grupo de tratamiento) probablemente fueron el resultado de la falta de cumplimiento en lugar de la resistencia, ya que se observaron periódicamente bajas concentraciones plasmáticas de VBR (datos no mostrados) y no se encontraron variantes conocidas de resistencia a los medicamentos. se encuentra en la proteína central o en la región de la transcriptasa inversa del gen de la polimerasa. Es importante destacar que, dado que VBR se está desarrollando para uso concomitante con NrtI, no se observaron interacciones farmacológicas clínicamente significativas entre VBR y ETV en los niveles de dosis estudiados.
Este estudio tiene varias limitaciones. No se utilizaron factores de estratificación para la asignación del tratamiento. En consecuencia, existen diferencias numéricas en las características basales de la enfermedad entre los subgrupos, con una interpretación limitada por el pequeño tamaño de la muestra. La exploración de estas diferencias potenciales con respecto a los resultados del tratamiento debería evaluarse en estudios futuros con un tamaño de muestra más grande. Aunque se demostró la supresión viral (evaluada tanto por el ADN del VHB como por el pgARN) y la tolerabilidad de VBR+ETV, la duración del tratamiento de 24 semanas puede no ser suficiente para demostrar el alcance total de la actividad antiviral o para revelar posibles EA que pueden surgir después de un tratamiento prolongado. tratamiento. En particular, los biomarcadores relacionados con el VHB (como HBcrAg, un biomarcador sustituto de la actividad transcripcional del cccDNA) pueden no mostrar cambios desde el valor inicial hasta que se establezcan cambios a más largo plazo en el cccDNA.
Estudios previos han demostrado que aunque la terapia antiviral puede reducir rápidamente el ADN del VHB a niveles indetectables, la disminución de HBcrAg puede retrasarse y tomar varios meses o años para alcanzar una magnitud similar de disminución. Es posible que tampoco se observen cambios en HBcrAg. debido al pequeño tamaño de la muestra en este estudio. Los pacientes de este ensayo pueden inscribirse en un estudio de extensión abierto (NCT03780543) y recibir VBR más NrtI durante un máximo de 148 semanas. Finalmente, como los pacientes tenían fibrosis hepática mínima y casi todos eran de ascendencia asiática con genotipo B o C del VHB, estos hallazgos no pueden normalizarse a una población global de pacientes con VHBc.
En resumen, 300 mg de VBR una vez al día más 0,5 mg de ETV no provocaron muertes ni eventos adversos que condujeran a la suspensión. Todos los TEAE y las anomalías de laboratorio fueron de grado 2 o menos en gravedad. No se observaron interacciones farmacológicas entre VBR y ETV, ni hubo evidencia de avance de resistencia en pacientes que cumplieron con el tratamiento. Cuando se agregó a ETV, la interferencia de los pasos adicionales en la replicación de VHB por VBR dio como resultado reducciones aditivas significativas en el ADN y pgRNA de VHB y mayores tasas de normalización de ALT en comparación con la monoterapia con ETV.
Fuente: journal-of-hepatology.eu
Referencia: https://doi.org/10.1016/j.jhep.2022.05.027
Artículo traducido y adaptado por ASSCAT