Actualización clínica de NASH: qué esperar en 2020
Revisión del panorama clínico de la esteatohepatitis no alcohólica (NASH, en sus siglas en inglés) en rápida evolución, con un resumen de todas las grandes novedades de 2019 y quién podría ganar la primera aprobación de medicamentos para NASH en 2020.
2020: ¿Un gran año en el desarrollo clínico de NASH?
La carrera ha estado en marcha durante algunos años para lograr el primer agente aprobado por la FDA para tratar la NASH. Esto podría llegar a buen término en 2020, ya que Intercept Pharmaceuticals presentó una nueva solicitud de medicamento para el ácido obeticólico (OCA) en 2019, y espera una decisión de la FDA en la primera mitad del año.
El resto de la competencia NASH sigue muy comprometida, y en esta publicación se revisarán los recientes desarrollos clínicos prometedores, así como varios fallos de alto perfil.
¿Por qué es tan importante un tratamiento para NASH?
NASH es un síndrome fibrótico inflamatorio que se desarrolla a partir de la enfermedad del hígado graso no alcohólico (NAFLD, en sus siglas en inglés). Los pacientes experimentan cicatrices progresivas hacia la cirrosis y potencialmente hepatocarcinoma. En las primeras etapas de la fibrosis, ésta es una trayectoria asintomática y se puede controlar o incluso revertir mediante cambios en la dieta y el ejercicio.
Sin embargo, las prevalencias globales de NAFLD y NASH se estiman en 25% y 35%, respectivamente, lo que significa que la intervención farmacológica tiene el potencial de generar retornos de inversión de gran éxito.
Más allá de la ausencia de una terapia aprobada y el tamaño del grupo de pacientes potenciales, NASH es una enfermedad intrigante para la investigación básica y de descubrimiento. Una variedad de mecanismos metabólicos, hormonales, inflamatorios y fibróticos interactúan en su desarrollo y progresión, presentando una variedad de ejes para el manejo y la resolución de la enfermedad. El campo de candidatos clínicos de 2019 ejemplifica la complejidad y riqueza de los objetivos terapéuticos.
Liderando el camino hacia NDA para terapias NASH
Intercept informó datos provisionales positivos de su ensayo Fase 3 REGENERATE de OCA, incluida la reunión del objetivo primario de mejorar la fibrosis hepática sin empeoramiento de NASH en 18 meses. Actualmente, OCA es la única terapia bajo investigación que cumple con uno de sus puntos finales primarios del estudio de Fase 3 en pacientes con NASH: mejora de la fibrosis sin empeoramiento de NASH. También es el único agente con una designación de terapia innovadora de la FDA para NASH con fibrosis. Estos resultados positivos llevaron a la compañía a presentar una revisión prioritaria para NDA.
OCA es un agonista semisintético de ácido biliar análogo de FXR, un importante regulador de los niveles de triglicéridos hepáticos. Persisten las preocupaciones sobre problemas de seguridad a largo plazo, incluido el aumento del colesterol circulante y los eventos cardiovasculares adversos. Estos pueden requerir la administración conjunta de estatinas. OCA también es un medicamento extremadamente costoso, que cuesta alrededor de 70.000 dólares al año cuando se prescribe para la indicación ya aprobada de colangitis biliar primaria. Estos factores están alentando a los competidores de Intercept a seguir adelante.
Se espera que el fabricante francés Genfit informe de datos provisionales de primera línea de su ensayo RESOLVEIT de Fase 3 en el primer trimestre de 2020. En noviembre, informó datos de seguridad positivos para elafibranor, incluida la falta de problemas con la hepatitis de interfaz. Esto le valió una recomendación para continuar. Elafibranor es un agonista dual de PPARα / δ que mejora el metabolismo de los triglicéridos y los lípidos.
Otros candidatos a fármacos de Fase 3 NASH
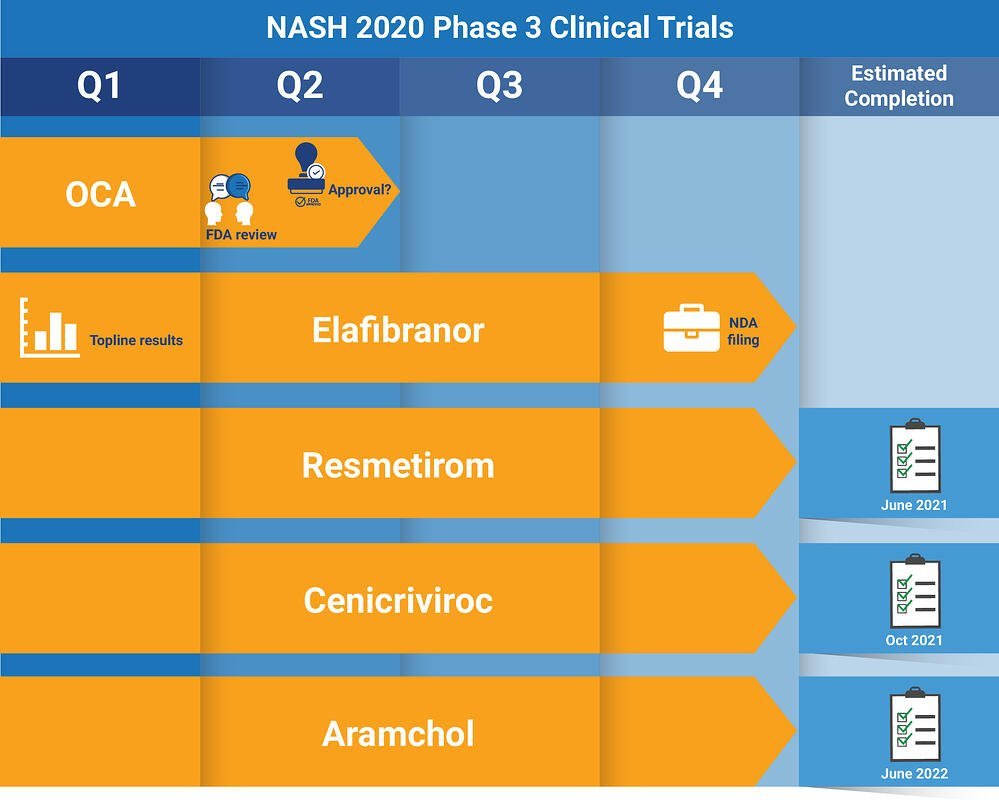
- Cenicriviroc: Allergan continuó el ensayo AURORA para la mejora de la fibrosis avanzada sin empeoramiento de NASH para este inhibidor del receptor CCR2 / CCR5. Se esperan resultados a principios de 2020.
- Aramchol: Galmed Pharmaceuticals inició su ensayo ARMOR fase 3/4 de 52 semanas en pacientes con NASH prediabético y diabético con fibrosis avanzada. Los puntos finales basados en la histología incluyen la resolución NASH sin empeoramiento de la fibrosis y la mejora de la fibrosis sin empeoramiento de la NASH. Aramchol es un modulador SCD1 dirigido al hígado de primera clase.
- Resmetirom: En diciembre, Madrigal Pharmaceuticals comenzó a dosificar a pacientes en un estudio de seguridad y biomarcadores de fase 3 en pacientes con NASH con fibrosis avanzada. En marzo, comenzaron su primer ensayo clínico de fase 3, con un punto final primario que es la resolución NASH. Resmetirom es el primer agonista beta del receptor de la hormona tiroidea de su clase.
Agentes candidatos para la fase 2 de NASH
Las aprobaciones potencialmente inminentes de OCA y elafibranor no han ahuyentado a numerosos participantes tardíos en la carrera de desarrollo de fármacos NASH.
- VK2809: Viking Therapeutics anunció el inicio de inscripciones para pacientes con EHNA con diversas etapas de fibrosis para un estudio de eficacia y tolerabilidad de fase 2b. Esto consiguió resultados positivos para la reducción de la grasa hepática en pacientes con NAFLD con buena seguridad en un ensayo de fase 2. VK2809 es otro agonista beta del receptor de la hormona tiroidea, y Viking lo describe como el “mejor en su clase”.
- Icosabutato: NorthSea inscribió a sus primeros pacientes con NASH para un ensayo de fase 2b de un ácido graso estructuralmente diseñado que regula las vías lipídicas fundamentales involucradas en la inflamación hepática.
- MSDC-0602K: En The Liver Meeting®, Cirius Therapeutics anunció datos positivos para marcadores no invasivos e histopatológicos del metabolismo y NASH para su sensibilizador de insulina moduladora de MPC. Cirius ahora planea reunirse con las autoridades reguladoras para discutir el diseño del estudio de Fase 3 planeado.
- Lanafibranor: Inventiva Pharma recibió la designación de vía rápida de la FDA para su agonista panPPAR. Los resultados de su prueba de Fase 2b NASH se esperan en H1 en 2020.
- Tropifexor y licoglifozina: Novartis informó datos prometedores de Fase 2 y 2a de 12 semanas, respectivamente, en The Liver Meeting. Estos incluyeron enzimas hepáticas mejoradas y niveles de grasa hepática en pacientes con NASH. Tropifexor es un agonista de FXR y la licoglifozina es un inhibidor de SGLT1 / 2.
- Aldafermin: La hormona humana diseñada por FGF19 de NGM Biopharmaceuticals, que interactúa con los receptores para regular la síntesis de bilis y la lipogénesis, continuó a través de pruebas de fase 2 multicohorte. NGM informó datos positivos para la reducción de la grasa hepática en pacientes inscritos en NASH.
- AKR-001: Akero Pharmaceuticals anunció la finalización de la inscripción para un ensayo de fase 2a utilizando otro análogo hormonal. Esto imita a FGF21, un importante regulador del metabolismo de lípidos y energía. El objetivo primario es la grasa hepática en pacientes con NASH.
- EDP-305: Enanta Pharmaceuticals informó que alcanzó los puntos finales primarios de la fase 2a en pacientes con NASH. El agonista FXR se queda atrás y se ve eclipsado por el desempeño histórico relativamente superior de OCA en pruebas similares.
No todos podemos ser NASHtronautas – Interrupciones del agente NASH en 2019
Hubo varias interrupciones de alto perfil de los aspirantes a la terapéutica NASH en 2019, que incluyen:
BI 1467335: Partners Pharmaxis y Boehringer Ingelheim abandonaron el curso de convertir su inhibidor SSAO / VAP1 en un medicamento NASH después de que se descubrieran interacciones no reveladas de medicamentos en la Fase 1.
- Firsocostat y cilofexor: Gilead probó su inhibidor ACC y agonista FXR, respectivamente: solos, en combinación entre sí y en combinación con su inhibidor ASK1 selonsertib (ver más abajo). Ninguno de los tratamientos redujo la cicatrización en un ensayo de fase 2 de pacientes con fibrosis NASH avanzada.
- Selonsertib: El fármaco de Gilead falló en dos ensayos de Fase 3, con un rendimiento tan bueno o peor que el placebo para reducir las mejoras histológicas de la fibrosis.
- Seladelpar: CymaBay Therapeutics finalizó los estudios de Fase 2b en su agonista PPARδ después de que las biopsias de pacientes indicaran la condición de hepatitis de interfaz. El medicamento tampoco había logrado reducir la grasa del hígado en los resultados preliminares del ensayo.
- Emricasan: Conatus Pharmaceuticals anunció que su inhibidor de pancaspasa asociado con Novartis fue superado por el placebo en la resolución de fibrosis en pacientes con NASH en un ensayo de fase 2b. Emricasan continuó su racha perdedora, habiendo fracasado en dos ensayos de enfermedad hepática de Fase 2b en 2018.
Predicciones de desarrollo de fármacos NASH
2019 fue nombrado el “Año de NASH”, pero nos enfrentamos a un curso más largo: años de NASH. Ya sea que elafibranor y OCA lleguen al mercado en 2020, se predice que la amplia variedad de objetivos de NAFLD/NASH y las poblaciones de pacientes que requieren diferentes tratamientos significa que el panorama clínico de NASH seguirá maduro en los años venideros.
Fuente: crownbio.com
