Mutaciones del virus de la hepatitis E: su importancia funcional y clínica
La infección por el virus de la hepatitis E (VHE) es una causa frecuente de hepatitis aguda y afecta a nivel mundial a más de 20 millones de personas, con tres millones de casos sintomáticos y 56.000 muertes reconocidas relacionadas con el VHE en todo el mundo.
El VHE es endémico en los países en desarrollo y está ganando importancia en los países desarrollados, debido al aumento en el número de casos autóctonos. En individuos inmunocompetentes, la replicación del VHE está controlada por el sistema inmune del huésped, pero se reconoce que algunos factores víricos (genotipos virales específicos y los mutantes) pueden modular la replicación y el curos de la infección del VHE. Existe un conocimiento limitado sobre como influyen las variantes genéticas del VHE a la patogénesis, la susceptibilidad y la respuesta terapéutica. Las variantes virales pueden modular estructuralmente las proteínas del VHE y, por lo tanto, desregular las interacciones entre el virus y el huésped. Esta revisión tiene como objetivo resumir el conocimiento y discutir los avances recientes en el papel casual de la heterogeneidad del VHE y sus variantes en la morfogénesis viral, la patogénesis, el resultado clínico y la resistencia antiviral.
Introducción
La infección por el virus de la hepatitis E (VHE) se está reconociendo cada vez más en la investigación médica, ya que la infección por el VHE ha llegado a los países industrializados. Aunque el VHE se descubrió en 1983 (Balayan et al., 1983) y se iniciaron análisis experimentales desde 1990/1991 (Reyes et al., 1990), existen lagunas en los conocimientos sobre las vías de transmisión, el ciclo vital, la patogénesis, la variabilidad genómica y la evolución viral.
Desde hace años, se producen epidemias importantes y brotes esporádicos de hepatitis E en los países tropicales y subtropicales (por ejemplo, en India, Uganda, Sudán y México), con decenas de miles de afectados (Dalton et al., 2013; Kamar et al. 2012). Aproximadamente dos mil millones de personas (un tercio de la población mundial) viven en áreas endémicas para el VHE y estarían en riesgo (Pérez-Gracia et al., 2013). Las infecciones por el VHE se documentan con menos frecuencia en los países industrializados, ya que se cree que están asociadas a viajes a países endémicos. Sin embargo, se han ido informando infecciones por VHE en Europa occidental (Dalton et al., 2013; Kamar et al., 2012; Pischke et al., 2014). Las razones de las discrepancias en la presentación del VHE entre países en desarrollo y países desarrollados son diversas. Es probable que se explique por diferencias en la ruta de transmisión y por la diferente distribución de los genotipos VHE (Pauli et al., 2015; Sayed et al., 2015). En los países en desarrollo, la infección por VHE se transmite principalmente por vía hídrica/fecal-oral debido a malas condiciones higiénicas, mientras que en los países desarrollados el VHE se transmite principalmente por consumo de carne y entrañas mal cocinadas (Mansuy et al., 2016). En este sentido, el VHE es único, ya que es el único virus de hepatitis con un reservorio animal.
Las variantes del VHE se sabe que están asociadas con la dinámica de transmisión y la patogenicidad (Kamar et al., 2012, 2014, Lee et al., 2016, Meng, 2011). Las mutaciones del VHE ocurren bajo la presión selectiva realizada por el sistema inmune del huésped y por los antivirales. La heterogeneidad del VHE contribuye a la diversidad en la patogénesis y los patrones de transmisión del VHE (Lhomme et al., 2014). En esta revisión, el objetivo es resumir los conocimientos y discutir los avances recientes en el papel de la heterogeneidad del VHE y sus variantes, en la morfogénesis viral, la relevancia clínica y la resistencia a los antivirales.
Curso clínico y patogénesis de la infección por VHE
Aunque la mayoría de las infecciones por el VHE son asintomáticas, el curso clínico de las infecciones sintomáticas incluye hepatitis E aguda y crónica, insuficiencia hepática fulminante y síntomas extrahepáticos (Debing et al., 2016a, Hoan et al., 2015). La hepatitis E aguda generalmente se define como una enfermedad autolimitada que dura aproximadamente 8 semanas y los síntomas son inespecíficos y casi indistinguibles de otros tipos de hepatitis viral aguda (Wedemeyer et al., 2012). El ARN del VHE puede detectarse tanto en el suero como en las heces antes del inicio de los síntomas clínicos y dura menos de un mes en el suero, después del inicio de los síntomas, pero puede persistir más tiempo en las heces (Krain et al., 2014). Se ha observado una forma grave de hepatitis aguda (insuficiencia hepática fulminante) en pacientes con enfermedades hepáticas preexistentes y en mujeres embarazadas (Dalton et al., 2007; Navaneethan et al., 2008). La gravedad de la infección por VHE en mujeres embarazadas puede estar asociada con el equilibrio hormonal y la complejidad inmunológica durante el embarazo (Bose et al., 2011; Navaneethan et al., 2008). La replicación del VHE que ocurre en la placenta humana puede conducir a complicaciones graves en las embarazadas, incluida la transmisión del VHE de la madre al recién nacido y el aborto (Bose et al., 2014; Navaneethan et al., 2008).
La hepatitis E crónica se define por la persistencia de ARN-VHE y/o IgM anti-VHE durante más de seis meses con niveles elevados de alanina aminotransferasa (ALT). La infección crónica por VHE se ha informado principalmente en individuos inmunocomprometidos, en receptores de trasplantes de órganos, pacientes sometidos a quimioterapia y pacientes infectados por el VIH (Dalton et al., 2009; Kamar et al., 2008). La hepatitis E crónica se ha asociado con el desarrollo de fibrosis y/o cirrosis en pacientes con trasplante de órgano sólido (Kamar et al., 2008). La infección crónica por VHE depende en gran medida de la respuesta inmune del huésped y, por lo tanto, la inmunidad suprimida en esos grupos específicos de pacientes permite que el virus persista y establezca una infección crónica. El deterioro de las respuestas de células T específicas del VHE probablemente esté asociado con el desarrollo de hepatitis E crónica (Suneetha et al., 2012). Sin embargo, también se han notificado casos raros de infección crónica y/o persistente por VHE en individuos sanos e inmunocompetentes (Gonzalez Tallon et al., 2011).
El VHE también puede contribuir a diversas manifestaciones extrahepáticas, como pancreatitis, trastornos hematológicos (trombocitopenia y anemia), trastornos renales y complicaciones neurológicas (síndrome de Guillain-Barré y meningoencefalitis) (Singh y Gangappa, 2007; Thapa et al., 2009; Wedemeyer et al., 2012). El descubrimiento de las cuasiespecies del VHE en el suero y el líquido cefalorraquídeo sugiere además un posible papel directo del virus en los trastornos neurológicos y se relaciona con la aparición de variantes neurotrópicas del VHE (Kamar et al., 2010). El mecanismo de las manifestaciones extrahepáticas se puede explicar por la replicación del VHE en los tejidos/órganos extrahepáticos y es causa de daño tisular local e inflamación. Esto es respaldado por hallazgos recientes, que mostraron la replicación del VHE en la placenta humana y en tejidos neuronales (Bose et al., 2014; Drave et al., 2016). Se han propuesto otros mecanismos, como respuestas inmunitarias de reacción cruzada, generación de complejos inmunes e infecciones secundarias (Feng, 2016). Sin embargo, el mecanismo subyacente exacto de las manifestaciones extrahepáticas del VHE precisa más investigaciones.
Biología del VHE y virología molecular
El VHE es un virus ARN pequeño, virus sin envoltura, de 32-34 nm de diámetro y que pertenece al género Orthohepevirus de la familia Hepeviridae (Kamar et al., 2012).
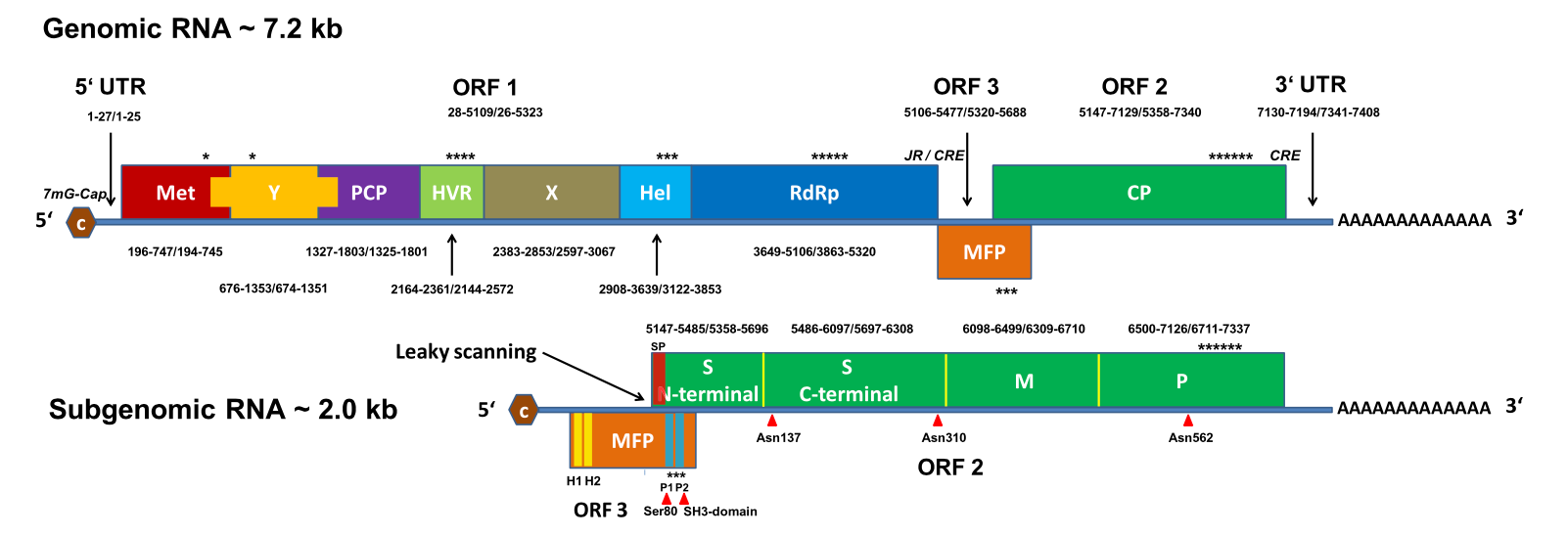
Figura 1. Descripción esquemática del genoma del VHE y las proteínas virales. La figura muestra el genoma lineal, ssRNA (+) del genoma VHE ~ 7.2 kb y las proteínas virales correspondientes. El extremo 5′ está tapado y el extremo 3′ está poliadenilado. ORF1 codifica la poliproteína no estructural, incluyendo metiltransferasa (Met), dominio Y (Y), cisteína proteasa tipo papaína (PCP), región hipervariable (HVR), macrodominio (X), ARN helicasa (Hel) y ARN dependiente ARN polimerasa (RdRp). ORF2 codifica la proteína de la cápside (CP), que contiene el dominio S (S), el dominio M (M) y el dominio P (P).
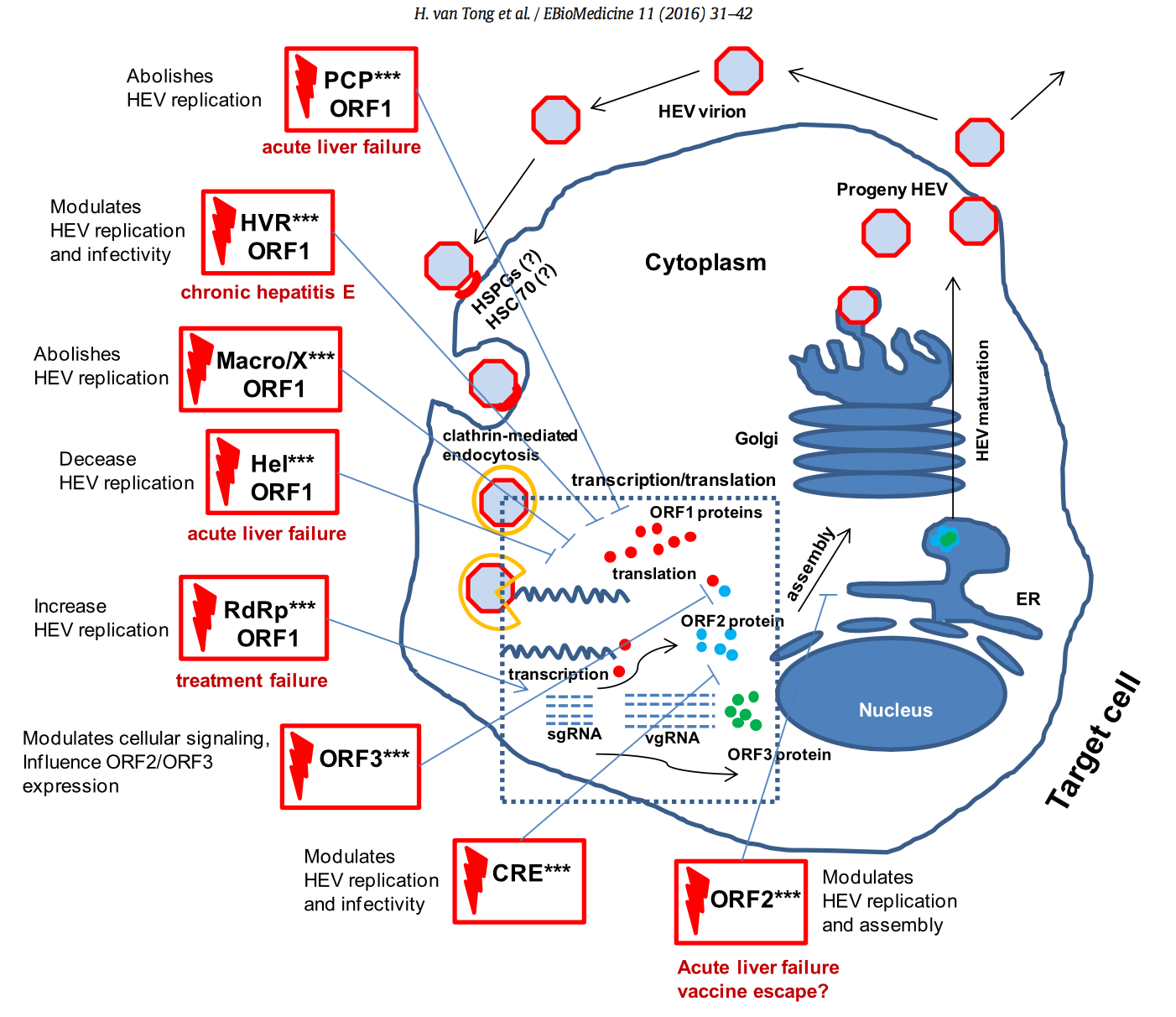
Aunque el ciclo vital del VHE es similar al de otros virus ssRNA, necesita más investigación (Fig. 2).
Variabilidad genética del VHE y la implicación clínica
Se reconocen siete genotipos del VHE dentro de la especie Orthohepevirus A basada en la filogenia de genomas virales completos (VHE-1 a VHE-7) (Smith et al., 2016). Cuatro genotipos del VHE (VHE-1 a VHE-4) son bien reconocidos como patógenos humanos, mientras que el VHE-5 y el VHE-6 se han identificado hasta ahora sólo en animales (jabalíes) (Smith et al., 2014). Recientemente, se ha informado que el camélido VHE-7 infecta a humanos y causa hepatitis E crónica, como se observa en un paciente trasplantado de hígado (Lee et al., 2016). Las cepas de los patógenos humanos incluyen VHE-1, VHE-2, VHE-3, VHE-4 y VHE-7 (Kamar et al., 2012, 2014, Meng, 2011). Además, cuatro de los principales genotipos del VHE patogénicos humanos se han clasificado en 24 subgenotipos, cinco subgenotipos de VHE-1 (1a a 1e), dos subgenotipos de VHE-2 (2a y 2b), diez subgenotipos de VHE-3 (3a a 3j) y siete subgenotipos de VHE-4 (4a a 4g) (Lu et al., 2006). Sin embargo, la subclasificación de los genotipos del VHE aún se halla en discusión, debido a la falta de datos validados.
Los genotipos del VHE tienen diferentes reservorios y distintos patrones de distribución y transmisión. El VHE-1 se distribuye con frecuencia en Asia, el VHE-2 en África y México, el VHE-7 en Oriente Medio, mientras que el VHE-3 y el VHE-4 están distribuidos por todo el mundo (Kamar et al., 2012; Lee et al., 2016; Rasche et al., 2016). El VHE-1 y el VHE-2 infectan exclusivamente a humanos, mientras que el VHE-3 y el VHE-4 tienen rango de huéspedes amplio (cerdos, jabalíes, conejos, venados y humanos) (Kamar et al., 2012, 2014; Meng, 2011). El VHE-7 puede infectar tanto a los camellos como a los humanos (Lee et al., 2016). El VHE zoonótico tiene el potencial de causar una enfermedad mortal en pacientes infectados y puede volverse más transmisible entre los humanos (Aggarwal y Jameel, 2011). El VHE-1 y el VHE-2 se transmiten principalmente a través de la vía hídrica/fecal-oral y son responsables de grandes brotes y epidemias transmitidas por el agua en países en desarrollo, mientras que el VHE-3, el VHE-4 y el VHE-7 están asociados con transmisión zoonótica y causan infecciones esporádicas en los países desarrollados (Kamar et al., 2012, 2014; Lee et al., 2016; Meng, 2011).
Se cree que los diversos genotipos del VHE están asociados con el curso clínico de las infecciones sintomáticas. El VHE-1 y el VHE-2 contribuyen principalmente a la hepatitis aguda grave, pero no a la infección crónica por VHE (Aggarwal y Jameel, 2011; Krain et al., 2014). Las infecciones con VHE-3, VHE-4 y VHE-7 no sólo causan hepatitis aguda, sino que también pueden conducir a hepatitis crónica en pacientes inmunocomprometidos (Geng et al., 2014; Geng et al., 2016; Lee et al., 2016). Rivero-Juárez et al., 2015). Los pacientes infectados con VHE-4 tuvieron resultados más graves en comparación con aquellos infectados con VHE-3 (Mizuo et al., 2005). La infección con VHE-1 pero no con VHE-3 y VHE-4 se asoció con formas graves de enfermedad hepática y complicaciones en mujeres embarazadas (Krain et al., 2014; Kumar et al., 2004). Además, se ha demostrado que la infección con VHE-3 causa insuficiencia hepática fulminante en pacientes con enfermedades hepáticas preexistentes (Dalton et al., 2007; Peron et al., 2007). Estos datos indican que la variabilidad del VHE contribuye significativamente a la patogénesis y la gravedad de la infección por VHE.
Figura 2. Efecto de las mutaciones en el ciclo de replicación del VHE y significado clínico. Descripción esquemática del ciclo de replicación del VHE y el efecto de las mutaciones que ocurren en el genoma del VHE (cuadros rojos, el dominio y la región están indicados) en la maquinaria transcripcional/traslacional (caja azul con puntos) del VHE. Los asteriscos (***) indican mutaciones conocidas. El posible efecto de las mutaciones en la replicación del VHE se indica y se describe su resultado clínico debajo de los recuadros rojos.
Recombinación del VHE
Los eventos de recombinación del VHE ocurren dentro de los siete genotipos del VHE definidos (Smith et al., 2014). Un estudio reciente caracterizó la PPR del genoma del VHE en 27 pacientes inmunocomprometidos con persistencia del VHE y 32 con la resolución de infecciones. De las 27 cepas aisladas de pacientes con persistencia del VHE, la recombinación se produjo en tres cepas del VHE durante el período de infección (Lhomme et al., 2014). Los eventos de recombinación aumentan la probabilidad de variabilidad genética y, por lo tanto, una evolución diferente con un potencial de cronificación de la infección por VHE (Nguyen et al., 2012). Además, se encontraron dos fragmentos de origen humano (inhibidor de la α-tripsina-ITI y tirosina aminotransferasa-TAT) insertados en la PPR. Esos fragmentos insertados mejoraron la replicación del VHE (Lhomme et al., 2014).
Mutaciones del VHE y su papel funcional
Los virus ARN exhiben una gran variabilidad genética por su evolución rápida, con una tasa de mutación estimada que varía de 10-6 a 10-4 sustituciones por nucleótido por copia (Sanjuan et al., 2010). Las tasas de mutación del VHE se estimaron indirectamente a partir de aislados clínicos como 1,5 sustituciones base por sitio por año y fueron similares a las informadas para los virus de la hepatitis C (Takahashi et al., 2004). Se han descrito mutaciones en todas las regiones: mutaciones en la región ORF1; mutaciones en la región ORF2; mutaciones en la región ORF3; mutaciones en la unión y elementos cis-reactivos (CRE).
Mutaciones del VHE y relevancia clínica, en especial en relación a las variantes relacionadas con la hepatitis fulminante
Algunas de las mutaciones del VHE descritas confieren propiedades diversas con cambios en el curso clínico de la enfermedad. Sin embargo, se desconoce la relevancia funcional y clínica de todas las variantes detectadas (Ray et al., 1992). Un análisis de 22 secuencias del VHE-4 de longitud completa de pacientes con hepatitis fulminante y aguda encontró que las sustituciones en las posiciones C1816 y U3148 se asociaron significativamente con la hepatitis fulminante (Inoue et al., 2006). Sin embargo, sólo se confirmó que la mutación U3148 estaba asociada con la hepatitis fulminante mediante un análisis adicional de 16 aislados del VHE-4. Análisis adicionales de 86 aislamientos del VHE mostraron que la variante U3148 tuvo una asociación más fuerte con la hepatitis fulminante en comparación con otras variantes (C3148 o G3148), y se asoció con una menor actividad de protrombina (Inoue et al., 2006). Un estudio comparable amplió los resultados usando 28 secuencias del VHE-4 de longitud completa (de hepatitis fulminante y aguda) e identificó a la variante C5907 como la más significativamente asociada con la hepatitis fulminante (Inoue et al., 2009). Un efecto adicional de las mutaciones U3148 y C5907 sobre la evolución fulminante de la hepatitis se confirmó mediante análisis de las secuencias completas de 28 muestras de VHE-4 y de 11 del VHE-3 aisladas, así como de 35 secuencias parciales (Inoue et al., 2009). Sin embargo, el mecanismo de cómo dichas mutaciones U3148 y C5907 influyen en la progresión de la hepatitis E no se ha resuelto.
La abundancia de mutaciones en el genoma del VHE, aislados de pacientes probablemente se deba a la presión inmune selectiva. Estas mutaciones permiten que el virus se adapte y module mejor la respuesta inmune del huésped lo que conduce a una mayor gravedad de las complicaciones.
Mutaciones y vacunación contra el VHE
La prevención de la infección por VHE en áreas endémicas se basa en la implementación de medidas higiénicas y sanitarias apropiadas para evitar la transmisión fecal-oral. En regiones donde la infección por el VHE es esporádica, se recomienda evitar el consumo de alimentos crudos. La infección por el VHE podría prevenirse con vacunas eficaces contra el VHE que de momento no están disponibles.
Relevancia clínica de las mutaciones del VHE en la terapia antiviral
Aunque no hay opciones de tratamiento específicas para el VHE con una actividad antiviral significativa, recientemente se ha documentado la efectividad del PEG-interferón-α en combinación con ribavirina o bien ribavirina sola frente al VHE (Kamar et al., 2014b; Peron et al. 2016; Wedemeyer et al., 2012). Sin embargo, se informó el fracaso del tratamiento con ribavirina en pacientes con hepatitis E crónica (Debing et al., 2014, 2016, Gisa et al., 2015; Lhomme et al., 2015; Todt et al., 2016).
Se han detectado mutaciones de resistencia antiviral (G1634R/K) que pueden ocurrir en el genoma del VHE bajo tratamiento con ribavirina, ya que se ha demostrado recientemente que la ribavirina causa mutaciones en el genoma del VHE y en otros virus ARN (Debing et al., 2016).
Los hallazgos recientes demuestran claramente el efecto mutagénico de la ribavirina en el genoma del VHE, lo cual puede conducir a la aparición de poblaciones virales distintas (Debing et al., 2014, 2016, Gisa et al., 2015; Todt et al., 2016). Estas poblaciones virales distintas resultantes del fracaso del tratamiento con ribavirina pueden causar un resultado clínico más complicado, y todo ello se halla en investigación.
En la práctica clínica, la exploración sistemática de las variantes genómicas del VHE por secuenciación de próxima generación debe considerarse para cualquier relevancia clínica, que puede asociarse con fracaso del tratamiento, infecciones crónicas y fulminantes para predecir los resultados de la terapia y la progresión de las enfermedades hepáticas.
Conclusiones y perspectivas
Aunque la infección por el VHE está ampliamente controlada por la respuesta inmune del huésped, la variabilidad genética del VHE, se asocia con variaciones en el curso clínico, la adaptación del huésped y las resistencias antivirales. Diferentes genotipos del VHE exhiben un rango de huéspedes selectivos con patrones de transmisión y patogénesis únicos. Las variaciones que se producen en el genoma del VHE pueden influir en la replicación del VHE y la interacción virus-huésped, y posteriormente pueden modificar la evolución. Bajo la presión inmune del huésped, pueden ocurrir mutaciones relevantes en todo el genoma del VHE, asociarse a formas graves de la enfermedad y a resistencias frente a los antivirales. Se precisan más estudios para dilucidar la contribución de las variantes del VHE en la fisiología, patogenia y evolución clínica del VHE.
Referencia: Hepatitis E Virus Mutations: Functional and Clinical Relevance Hoang van Tong et al. (agosto 2016) EBioMedicine 11 (2016) 31–42
Artículo traducido y adaptado por ASSCAT

