Hígado graso no alcohólico y la coordinación entre atención primaria y secundaria
La enfermedad del hígado graso no alcohólico (NAFLD, en sus siglas en inglés) tiene una prevalencia del 25% al 30% en poblaciones no seleccionadas y se ha convertido en la razón principal de las visitas a servicios de hepatología.
Desde la perspectiva de la enfermedad hepática, la NAFLD tiene una alta prevalencia pero baja severidad. Los estudios de detección en personas con riesgo de NAFLD han demostrado una prevalencia de fibrosis avanzada en el 5%, lo que subraya la necesidad de vías sólidas para la estratificación del riesgo en la atención primaria, con referencias posteriores según sea necesario. En esta revisión, se explica la coordinación entre la atención primaria y la secundaria en relación a la estratificación de riesgos y el manejo de los pacientes con NAFLD. Nos centraremos en temas seleccionados de epidemiología e historia natural y comentaremos la carga de la enfermedad en la atención primaria, la evidencia sobre la detección de NAFLD, la justificación de las pruebas para detectar fibrosis avanzada y el manejo óptimo de la enfermedad en la atención primaria.
Introducción
La enfermedad del hígado graso no alcohólico (NAFLD, en sus siglas en inglés) tiene una prevalencia del 25% al 30% en la población general y se ha convertido en el principal motivo de derivación a los servicios de hepatología. Se espera que el número de pacientes diagnosticados con NAFLD y referidos aumente, debido tanto a la creciente epidemia de obesidad y diabetes, como a la creciente conciencia de la enfermedad.
La NAFLD es una enfermedad sistémica, aunque a menudo, se percibe como una manifestación hepática intrascendente del síndrome metabólico. Si bien algunos pacientes desarrollarán una enfermedad hepática progresiva que puede conducir a cirrosis y cáncer de hígado, la mayoría de los afectados nunca desarrollarán complicaciones hepáticas. De hecho, la enfermedad cardiovascular es la principal causa de mortalidad en los pacientes con NAFLD, seguida por cáncer extrahepático. Debido a la alta prevalencia y a la baja gravedad de la NAFLD, es crucial que los médicos de atención primaria participen activamente en la detección y el tratamiento de los pacientes ambulatorios e identifiquen a los pacientes con riesgo de enfermedad hepática para derivación a los especialistas, y también es crucial la educación adecuada para los médicos de atención primaria sobre el seguimiento y el tratamiento de los pacientes considerados de bajo riesgo. En esta revisión, se explica la coordinación entre la atención primaria y especializada con respecto a la estratificación de los riesgos de complicaciones y el manejo de pacientes con NAFLD. Se enfocan temas seleccionados de epidemiología e historia natural, y se comenta la carga de la enfermedad en la atención primaria, la evidencia para la detección de NAFLD, la justificación para la prueba de fibrosis avanzada y el manejo óptimo de la enfermedad en el entorno de la atención primaria. Esta revisión es relevante para los equipos de atención primaria y especialistas involucrados en el diagnóstico inicial de NAFLD y el tratamiento de las personas con mayor riesgo de desarrollar NAFLD. El enfoque en la detección y las pruebas también es relevante para los clínicos especialistas que desarrollan servicios para NAFLD. Además, se subrayan áreas de incertidumbre y necesidades para futuras investigaciones.
Epidemiología
La NAFLD es una entidad global cada vez más común que se define por la presencia de esteatosis hepática y diversos grados de lesión hepática y fibrosis, que se producen en ausencia de cualquier otro factor etiológico, como el exceso de alcohol. La aparición de NAFLD en los últimos 20 años ha sido impulsada por el dramático aumento en los niveles globales de obesidad y diabetes tipo 2, con los cuales la NAFLD está estrechamente vinculada.
Los estudios epidemiológicos han utilizado diferentes criterios para el diagnóstico de la NAFLD, por lo que las prevalencias resultantes dependen de los estudios. En general, los estudios que se requieren para hacer el diagnóstico de EHGNA, la analítica hepática esté alterada, han reportado estimaciones de prevalencia mucho más bajas en comparación con los estudios que utilizan métodos de imagen. Se ha observado y está plenamente aceptado, que los pacientes con EHGNA, e incluso aquellos con daño hepático sustancial, pueden tener la analítica del hígado completamente normal, pero ello ha obstaculizado la investigación clínica. Además, EHGNA comprende un amplio espectro de la enfermedad, se refiere tanto a pacientes con una esteatosis simple (leve), a casos con inflamación progresiva, a pacientes con esteatohepatitis no alcohólica (NASH) y enfermos con fibrosis que progresan a cirrosis. Debido a que la distinción entre enfermedad leve y más progresiva a menudo requiere investigaciones adicionales, incluidos procedimientos invasivos (por ejemplo, biopsia hepática), existen pocos datos sobre la prevalencia real de NASH y fibrosis progresiva. Esta escasez de datos es relevante porque se ha reconocido que las complicaciones relacionadas con la enfermedad hepática surgen sólo después de muchos años y ocurren principalmente en personas con NASH y fibrosis.
Los datos de prevalencia global de NAFLD y NASH han sido revisados por Younossi y colegas, en 86 estudios, de 22 países y que abarcan 8,515.431 pacientes, establecieron una prevalencia global de NAFLD del 25,24%, hallaron la mayor prevalencia en el Medio Oriente y Sudamérica. Sin embargo, las prevalencias en las diferentes regiones geográficas fueron muy similares, con una prevalencia por edad después de los 40 años y que seguía aumentando después de los 70 años. La prevalencia general combinada de NASH en pacientes con NAFLD fue de 59,10%, sin embargo, extrapolar este valor a la prevalencia de la población de NASH es difícil debido a sesgos inherentes ya que muchos datos se generan en los centros especializados. En relación a los resultados obtenidos con el modelo que analizan, una vez más de Younossi y colegas, sugirieron una prevalencia de NASH era del 2% al 5% en Estados Unidos y en los principales países europeos.
Finalmente, los datos sobre la prevalencia de EHGNA con fibrosis avanzada son aún escasos, pero de gran importancia clínica. Los estudios de base poblacional han reportado prevalencias más bajas que los de los centros especializados, este sesgo se confirma al analizar los estudios de los centros de referencia. No obstante, las cifras sugieren de forma conservadora una prevalencia de 0,3%-1,0% para NASH con fibrosis avanzada en EEUU y Europa.
Historia natural
La progresión del daño hepático en el contexto de NAFLD o NASH no se comprende completamente, puesto que se depende de la biopsia hepática para explorar los cambios en la lesión hepática. Además, la mayoría de los resultados analizados que se informaron fueron comunicados por los investigadores en estudios de un solo centro y en unidades especializadas, donde se realizaron biopsias repetidas, en relación a eventos clínicos. Esto produce un sesgo inevitable, porque las biopsias repetidas se realizan impulsadas, en muchos pacientes, por preocupaciones clínicas, lo cual proporciona un diagnóstico individual pero no una comprensión clínica que no es representativa de la tasa general de progresión de la enfermedad. Singh y sus colegas analizaron la tasa de progresión de la fibrosis histológica (a estadios más avanzados de la enfermedad) en adultos con NAFLD y encontraron que la tasa de progresión varía según la gravedad de la enfermedad basal. En los pacientes con una enfermedad en principio más leve, el progreso pareció ser más lento, mientras que en los pacientes con NASH ya desde el inicio del estudio, la fibrosis progresó más rápidamente. Estos resultados son útiles para informar en general, pero se debe tener en cuenta que todas las tasas de progresión fueron aún lentas. El tiempo necesario para avanzar en un estadio de la fibrosis hepática fue de 7 años, en la enfermedad de progresión rápida (NASH) versus 14 años en la enfermedad de progresión lenta (NAFLD).
El método para evaluar los cambios en la fibrosis en pacientes con NASH merece consideración. La fibrosis se evalúa comúnmente mediante el uso de la clasificación establecida por la NASH Clinical Research Network (CRN), que clasifica la fibrosis de F0 a F4, dependiendo del patrón histológico observado. Aunque es útil, este sistema tiene algunos fallos. La fibrosis se clasifica categóricamente, pero se analiza como si fuera una variable continua. Además, el sistema de estadificación no es lineal, con diferencias absolutas en la deposición de colágeno que son modestas entre las etapas más tempranas y más marcadas en las etapas posteriores. Estas diferencias en la estadificación son relevantes para la revisión sistemática por Singh y colegas, en la cual la mayoría de los pacientes tenían fibrosis en etapas tempranas y, por lo tanto, las diferencias reportadas representan cambios relativamente pequeños en la progresión de la fibrosis. Además, estos estudios también mostraron en algunas personas cierta mejoría espontánea de la fibrosis en estas primeras etapas de NASH, destacando la naturaleza dinámica de la enfermedad.
Singh y sus colegas realizaron análisis estadísticos complejos para comprender qué factores podrían predecir el cambio histológico. Se demostró que varias características predecían la progresión pero solamente la hipertensión arterial sería un factor predictivo. Este resultado, creen que podría representar un hallazgo casual, pero en su opinión merece más estudios.
Se ha establecido con evidencias que las causas principales de morbilidad y mortalidad, en pacientes con NASH, son las enfermedades cardiovasculares y las neoplasias no hepáticas. Dado que en los pacientes con NASH coexiste con frecuencia el síndrome metabólico (asociado con un mayor riesgo de enfermedad cardiovascular y cáncer), estos resultados no son sorprendentes. Este conocimiento es particularmente relevante para el manejo compartido de tales pacientes en atención primaria, en los que se debe realizar un seguimiento del síndrome metabólico. La identificación de los factores que predicen el desarrollo de la mortalidad general y relacionada con el hígado ha sido el foco de muchos estudios, con la conclusión de que los factores metabólicos, como la diabetes y el uso de las estatinas, son factores pronósticos importantes. De manera similar, varios estudios han informado que la existencia y gravedad de la fibrosis hepática es un predictor potente de la mortalidad general y relacionada con el hígado.
El vínculo entre la fibrosis hepática y la mortalidad relacionada con el hígado es de esperar, y confirman los resultados presentados por Dulai y colegas que sugirieron que el riesgo de mortalidad se manifiesta después del desarrollo de una mayor fibrosis hepática (desde el estadio F2) y aumenta exponencialmente a partir de entonces. El vínculo entre la fibrosis hepática y la mortalidad general comienza en etapas precoces de fibrosis y aumenta directamente según la gravedad de la fibrosis. Esta relación entre fibrosis y mortalidad general podría atribuirse a la presencia ciertos factores metabólicos que conducen a la fibrosis y no a la fibrosis en sí misma, aunque sigue habiendo una discusión sobre el papel directo de la NASH en el riesgo cardiovascular una vez que se controlan los factores del síndrome metabólico concomitante.
Otros estudios que han resaltado el vínculo entre la fibrosis y los resultados clínicos han mostrado resultados discrepantes. Se postula que en el diagnóstico definitivo de la EHGNA, el sello distintivo de la lesión hepática es el balonamiento del hepatocito que, en presencia de factores concomitantes (por ejemplo, esteatosis), es un activador reconocido de la fibrosis hepática. Sin ser demasiado dogmático, este es el paradigma aceptado por el cual la lesión hepática produce fibrosis, independientemente de la naturaleza del daño hepático, aunque con advertencias que incluyen el efecto fibrogénico directo de algún tipo de grasa, como el colesterol libre. El diagnóstico de certeza de NASH en ocasiones y aún después de la biopsia, es incierto, se ha de tener en cuenta que NASH es una entidad más dinámica que la fibrosis, y es probable que la inflamación sea el principal impulsor de la progresión de la fibrosis. Además, la rapidez en la progresión de la fibrosis es muy variable y el depósito de grasa es probable que sea sólo uno de los factores de riesgo que inciden en la fibrosis hepática y, por lo tanto, en los resultados clínicos.
Diagnóstico de EHGNA en atención primaria
En ausencia de un cribado de la población, el diagnóstico de EHGNA en la atención primaria generalmente se produce al observar alteraciones en la analítica del hígado o por la detección de la esteatosis en una ecografía o TAC realizados por otra indicación. Los análisis de sangre del hígado a menudo se solicitan en la atención primaria como un control clínico general. Por lo tanto, los médicos de atención primaria a menudo se enfrentan a pruebas anormales del hígado sin tener síntomas clínicos. La investigación adicional de una causa subyacente y la gravedad de la enfermedad hepática, a menudo dependerá del grado de alteración detectado. Aunque este enfoque es apropiado cuando se hace referencia a marcadores de la síntesis hepática, como la albúmina y el tiempo de protrombina, no lo es tanto cuando se relaciona con enzimas hepáticas (ALT, AST, GGT), ya que puede existir una enfermedad hepática en el contexto de concentraciones de enzimas hepáticas séricas normales o mínimamente anormales. Por lo tanto, a menos que exista una causa transitoria obvia, como una sepsis o la prescripción temporal concomitante de medicamentos, el foco debe centrarse en la causa subyacente de la enfermedad.
Un análisis de la causa de los análisis de sangre hepáticos anormales en atención primaria indicó que la mayoría son causados por EHGNA o por exceso de alcohol, y en una elevada proporción no se halla una causa discernible. Si bien los casos sin causa discernible pueden deberse a enfermedades transitorias, también pueden reflejar un bajo consumo de alcohol o EHGNA con esteatosis no diagnosticada por la ecografía. En una cohorte de atención primaria de más de 1.000 pacientes con diagnóstico incidental de pruebas hepáticas anormales, la EHGNA fue la causa subyacente en el 26% de los casos, mientras que no se identificó la causa en el 45% de los casos. Para los pacientes diagnosticados de EHGNA, la derivación a los especialistas del hospital ha sido diversa, así puede suceder que casos de enfermedad hepática avanzada se pasan por alto, y pacientes con enfermedad mínima se refieren para la atención secundaria. Se requiere una respuesta sistemática a los análisis de sangre hepáticos anormales para estandarizar el abordaje para tales pacientes. Este diagnóstico diferencial, debería incluir las pruebas de hepatitis B y C y de enfermedad hepática autoinmune, ferritina sérica y saturación simultáneas, concentraciones de alfa-1-antitripsina, ceruloplasmina sérica (en pacientes menores de 40 años), una ecografía abdominal y una historia detallada del consumo de alcohol y de la medicación concomitante.
Selección de pacientes con EHGNA en atención primaria
Aunque no se justifica la detección de EHGNA en poblaciones no seleccionadas, la detección selectiva en grupos que se consideran en alto riesgo de padecer la afección sigue siendo un tema polémico, según reflejan las guías clínicas de las principales sociedades científicas y organismos encargados de la puesta en marcha. Faltan datos sobre la progresión de la enfermedad y los resultados a largo plazo en poblaciones no seleccionadas, la ausencia de una prueba de detección óptima así como la falta de terapias efectivas específicas de la enfermedad, dificulta realizar análisis de coste-efectividad en los enfoques de detección en EHGNA.
Los métodos de imagen no invasivos y los biomarcadores séricos están disponibles para el diagnóstico de EHGNA y se podrían usar como parte de las estrategias de detección dirigidas. La resonancia magnética (ya sea con imágenes de fracciones de densidad de protones o con espectroscopia) es el estándar de oro para el diagnóstico de EHGNA en centros de investigación, pero, debido a la falta de accesibilidad y a los costes, este método no es actualmente viable para uso clínico. La ecografía abdominal sólo puede detectar la esteatosis cuando supera el 20%-30% de los hepatocitos afectados y, por lo tanto, los pacientes con EHGNA y un grado de esteatosis de entre el 5% y el 20%, no se detectarán. En estos casos la ecografía tiene el beneficio de la visualización directa del hígado, y la posibilidad de diagnosticar patologías adicionales, como las lesiones hepáticas. El parámetro de atenuación controlada (CAP) del FibroScan® (un método de elastografía por ultrasonido; Echosens, París, Francia) puede identificar la esteatosis con una sensibilidad y especificidad razonables. En un metanálisis de casi 4.000 pacientes, el área bajo la curva para la identificación de cualquier grado de esteatosis fue 0,82, con un corte de 248 dB/m, mientras que el área para la identificación de un grado de esteatosis de más del 33% fue de 0,86, con un corte de 268 dB/m.
En particular, los valores de la CAP se vieron influenciados por la causa subyacente de la enfermedad hepática y la presencia de diabetes. También vale la pena señalar que no hay métodos de CAP estandarizados para el uso de la sonda XL del FibroScan® en pacientes obesos. Los algoritmos disponibles para la EHGNA y basados en biomarcadores séricos incluyen el índice de hígado graso (FIS), el índice de grasa hepática NAFLD, el índice de esteatosis hepática y el Steatotest. Aunque estas pruebas son útiles para estudios de investigación basados en la población, son menos útiles para la detección individual, debido a un número relativamente alto de resultados falsos positivos. En general, la especificidad subóptima es un problema para todos los métodos disponibles para la detección de EHGNA.
El diagnóstico de NASH tiene más relevancia clínica que el diagnóstico de EHGNA con esteatosis simple, pero igualmente se ve obstaculizado por la ausencia de métodos no invasivos con una precisión diagnóstica adecuada. Los fragmentos circulantes de la citoqueratina-18 (queratina, citoesqueleto 18 tipo I), que es un marcador apoptótico, es el biomarcador más estudiado para la NASH, pero este método tiene una baja sensibilidad y no se correlaciona con el balonamiento, que es el sello histológico de NASH.
Las pautas publicadas conjuntamente por las Asociaciones Europeas para el Estudio del Hígado (EASL, en sus siglas en inglés), de la diabetes y de la obesidad abogan por la identificación de casos de NAFLD mediante el uso de una ecografía abdominal en personas con obesidad, diabetes tipo 2, síndrome metabólico o con un hallazgo incidental de concentraciones anormales de aminotransferasas. Estas organizaciones científicas abogan por añadir el resultado de la ecografía a los algoritmos basados en biomarcadores séricos debido a la información adicional que puede proporcionar una ecografía. También abogan por una evaluación integral de la enfermedad asociada a EHGNA en aquellos pacientes con un diagnóstico incidental de esteatosis.
Las directrices de la Asociación Americana para el Estudio de la Enfermedad Hepática (AASLD, en sus siglas en inglés) no recomiendan el examen de rutina en grupos de pacientes de alto riesgo o cualquier investigación adicional de la esteatosis incidental, a menos que haya evidencia de enfermedad crónica del hígado o pruebas anormales del hígado (que ya sugiere un alto grado de sospecha para los pacientes con diabetes tipo 2), pero sin recomendaciones específicas para un enfoque de diagnóstico o monitoreo en estos pacientes.
Las directrices de la Sociedad Británica de Gastroenterología sobre pruebas de sangre anormales en el hígado, publicadas en 2018, tampoco recomiendan la detección de EHGNA hasta que haya más evidencia disponible sobre la rentabilidad.
El Instituto Nacional para la Excelencia Clínica (NICE, en sus siglas en inglés) del Reino Unido realizó un análisis de coste-efectividad para la detección de EHGNA en la población general. Los costes se estimaron para un ciclo de vida y se asumió un ciclo de reevaluación de 6 años para EHGNA. La progresión de EHGNA en el modelo se separó como EHGNA sin fibrosis avanzada, EHGNA con fibrosis avanzada y cirrosis. El programa de referencia NHS 2013-2014 se utilizó para el cálculo del coste relevante. El caso base para la prueba de la esteatosis hepática EHGNA, fue una persona de 45 años con diabetes tipo 2 o síndrome metabólico. Se compararon varias pruebas para la detección de más del 5% y más del 30% de la esteatosis hepática. El análisis mostró que la detección de EHGNA era rentable en comparación con ninguna detección, siendo el índice de hígado graso (FIS) la prueba más rentable, seguida de una ecografía abdominal.
Debido a que la prueba del FIS tenía intervalos de confianza amplios para la sensibilidad lo cual podría resultar en un alto número de falsos positivos, NICE no recomendó la detección de EHGNA. Corey y sus colegas realizaron un análisis de coste-efectividad ligeramente diferente. Este último modelo asumió un ciclo de seguimiento de por vida. Los costes médicos y de los procedimientos se extrajeron de las tasas de reembolso de Medicare, y se asumieron costes anuales separados según el estado de salud para NASH sin cirrosis, cirrosis compensada y cirrosis descompensada. Este análisis asumió que un paciente de 50 años de edad con diabetes tipo 2 era el caso base y seleccionó una ecografía para el diagnóstico de EHGNA, seguido de una biopsia de hígado si el resultado era positivo. Los pacientes diagnosticados con NASH fueron tratados con pioglitazona. Se estableció un 21% de diagnóstico incidental de NAFLD en el análisis de costes en el grupo no evaluado. El estudio concluyó que la detección no era rentable, principalmente debido a la disminución en la calidad de vida debido a los efectos secundarios de la pioglitazona.
Es importante considerar la carga de la enfermedad hepática avanzada que se pasa por alto si los pacientes en riesgo, no son examinados para detectar EHGNA y, posteriormente, para detectar la presencia de fibrosis hepática avanzada. Es bien sabido que la gravedad de la enfermedad hepática en la EHGNA es independiente del aumento de los valores de alanina aminotransferasa y, de hecho, todo el espectro histológico de EHGNA se puede observar en pacientes con valores normales de ALT. En el estudio de Rotterdam, donde se incluyó a más de 3.000 participantes mayores de 45 años, la prueba de detección de FibroScan® mostró que el 5,6% de los participantes tenían una probable fibrosis clínicamente relevante, y ésta se asociaba a la esteatosis y a la diabetes tipo 2. En un estudio de Hong Kong, con casi 2.000 pacientes con diabetes tipo 2 y sin antecedentes de enfermedad hepática crónica, se encontró un aumento de las mediciones de la rigidez hepática (que indica fibrosis) en 17,7% de los pacientes. De los 94 pacientes que tuvieron una biopsia hepática posterior, el 50% tenía fibrosis avanzada o cirrosis.
Un estudio llevado a cabo en el Reino Unido, realizado en 919 pacientes con riesgo de enfermedad hepática crónica en cuatro centros ambulatorios, demostró que el 25,6% de los pacientes tenía una rigidez hepática avanzada y el 2,9% tenía cirrosis confirmada, con obesidad, diabetes tipo 2, y abuso de alcohol como principal factor de riesgo. En una revisión sistemática de pruebas no invasivas para estratificar a pacientes con riesgo de enfermedad hepática avanzada en un entorno de población general, la prevalencia de fibrosis avanzada varió de 0% a 2,7%, según las características de la población. Se encontraron analíticas hepáticas normales en aproximadamente el 50% de los pacientes con fibrosis avanzada o cirrosis.
Por lo tanto, aunque la detección de EHGNA no se recomienda universalmente, existe una posible justificación para la detección selectiva en grupos de riesgo en lugar de confiar en el diagnóstico incidental al hallar pruebas hepáticas alteradas o hígado graso en las ecografías. Dadas las limitaciones de los métodos de detección existentes para la presencia de EHGNA, la búsqueda directa de fibrosis en pacientes de alto riesgo podría ser una alternativa a explorar. Una colaboración sólida entre la atención primaria y especializada es importante para el diseño de protocolos para las pruebas y la derivación; la efectividad clínica de tales protocolos deberá probarse en estudios prospectivos. El grupo que recibe placebo en los ensayos aleatorizados y controlados que están en curso proporcionará datos importantes sobre la historia natural de la EHGNA y ayudará a definir mejor los modelos de coste-efectividad. La llegada de tratamientos farmacológicos efectivos también hará que el diagnóstico de EHGNA sea más relevante para médicos y pacientes.
Prueba de fibrosis avanzada
Aunque la detección de EHGNA es polémica, en todas las guías recientes se recomendó una prueba de fibrosis avanzada (F3 en el sistema de estadificación NASH CRN) en pacientes con diagnóstico establecido de EHGNA. De hecho, la presencia de fibrosis avanzada es el factor más importante que determina los resultados clínicos en pacientes con EHGNA. Sería deseable apuntar a pacientes con fibrosis establecida (F2 en el sistema de estadificación NASH CRN) para las estrategias de prueba debido al mayor riesgo de progresión; sin embargo, esto no es posible en la actualidad debido a la precisión diagnóstica subóptima de las pruebas no invasivas existentes para la fibrosis en el estadio F2. La puntuación de fibrosis NAFLD (NAFLD Fibrosis Score) y la puntuación de fibrosis-4 (FIB-4) son pruebas no invasivas bien validadas y simples que tienen un alto índice de probabilidad negativa para la exclusión de la fibrosis avanzada. Es importante destacar que los pacientes con valores inferiores a la normalidad en estas pruebas tienen excelentes pronósticos relacionados con el hígado, durante 10 años de seguimiento. Suponiendo una prevalencia de fibrosis avanzada de menos del 5% en pacientes no seleccionados con EHGNA, el valor predictivo negativo de estas pruebas es de más del 98%.
Figura: Un algoritmo de pruebas de dos pasos para la fibrosis avanzada en atención primaria. Los porcentajes que aparecen en la figura se basan en una prevalencia de fibrosis avanzada del 5% y en la precisión diagnóstica de las pruebas no invasivas.
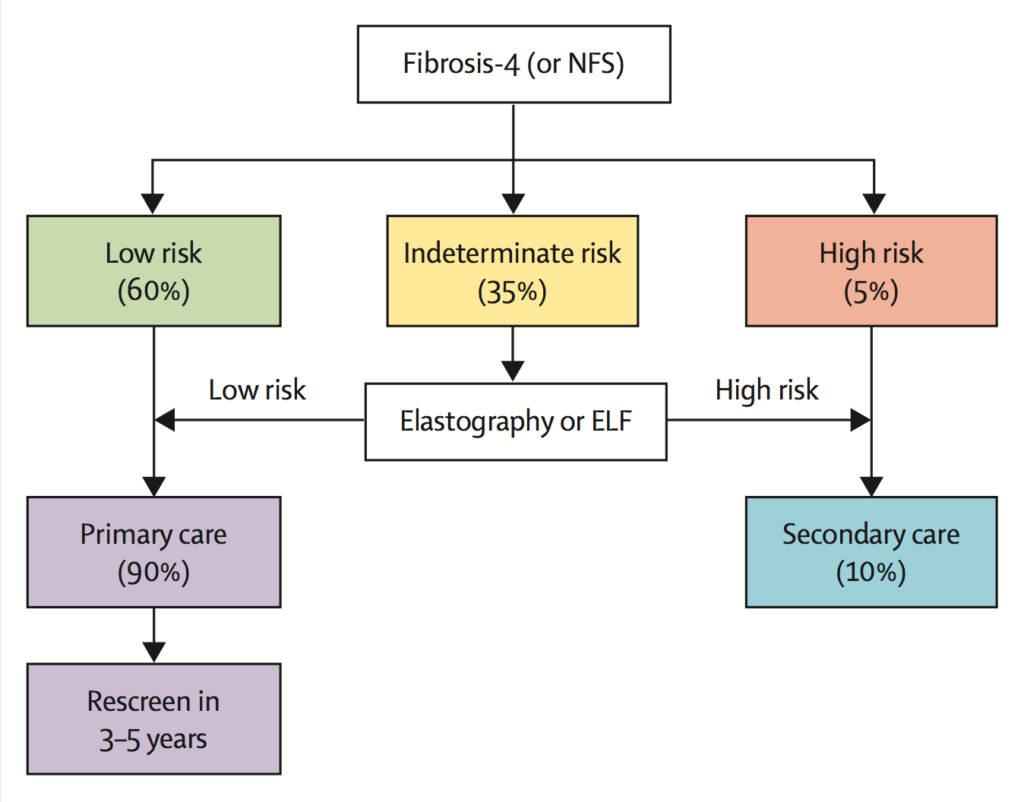
La puntuación FIB-4 consta de menos variables y, por lo tanto, es más sencillo de calcular e incorporar en la atención primaria para el diagnóstico y seguimiento de pacientes; esta puntuación también funciona ligeramente mejor que el NFS en las comparaciones de persona a persona. Estas pruebas tienen una doble normalidad, el valor bajo para excluir un diagnóstico y el valor alto para diagnosticar la presencia de fibrosis avanzada. Dado que los algoritmos se desarrollaron a partir de resultados de biopsias hepáticas de pacientes menores de 65 años, los valores de ambas puntuaciones deben ajustarse para las personas mayores de 65 años, para tener en cuenta la ponderación inadecuada de la edad. Una proporción de pacientes, aproximadamente el 40%-50%, se clasifica en una categoría indeterminada entre los dos valores cutáneos y requiere pruebas adicionales. Por lo tanto, se requiere una estrategia de pruebas a dos niveles para casi la mitad de los pacientes que se controlan en atención primaria. La elección de la prueba de segundo nivel podría ser una técnica de elastografía o un algoritmo sérico patentado (según la disponibilidad y experiencia locales).
Tabla 1: Pruebas de fibrosis no invasiva más ampliamente disponibles para fibrosis avanzada en pacientes con enfermedad de hígado graso no alcohólico (NAFLD). La fibrosis avanzada categorizada como etapa 3 en la clasificación de la Red de Investigación Clínica de Esteatohepatitis No Alcohólica. El valor predictivo negativo (VAN) se basa en una prevalencia de fibrosis avanzada del 5%. Los datos de precisión diagnóstica se derivan de Crossan y colegas.

Tabla 2: Manejo de atención primaria de pacientes con enfermedad del hígado graso no alcohólico (NAFLD), por comorbilidad.

FibroScan® es la técnica de elastografía más ampliamente disponible, con una validación adecuada en EHGNA en cohortes europeas y americanas. La introducción de la sonda XL ha permitido que la técnica se realice en pacientes obesos y ha abordado en gran medida la alta tasa de fracaso previo (debido a la obesidad) que se veía con la sonda M estándar en pacientes con EHGNA. Menos del 5% de los exámenes con la sonda XL fallan o muestran resultados poco fiables en manos de operadores experimentados, como se informó en una auditoría de más de 1.500 exámenes. La elastografía por resonancia magnética es superior a otras técnicas de elastografía para estadios de fibrosis más baja, pero tiene una precisión diagnóstica similar a la de la fibrosis avanzada. La técnica está disponible sólo en centros especializados y, por lo tanto, no es adecuada para fines de detección.
Existen varias pruebas séricas patentadas que se desarrollaron principalmente en cohortes de pacientes con infección crónica por hepatitis C, incluyen: FibroTest, el ELF (prueba de fibrosis hepática mejorada), Hepascore y FibroMeter. Tanto la puntuación ELF como el FibroMeter han sido validados en pacientes con EHGNA.
Las pautas de la EASL recomiendan el uso de pruebas de fibrosis no invasivas para descartar una fibrosis avanzada en pacientes con EHGNA y concentraciones normales de aminotransferasas, aunque no se recomienda ningún algoritmo específico. Las directrices abogan además por una referencia directa a un especialista en hígado en pacientes con concentraciones anormales de aminotransferasas y sin una evaluación previa no invasiva de fibrosis. Se debe tener en cuenta que esta recomendación de referencia es sólo para personas con factores de riesgo cardiometabólico y está destinada a la atención secundaria o terciaria no hepatológica en lugar de la atención primaria. Las pautas de la AASLD establecen que el score NFS y el FIB-4 son herramientas clínicamente útiles para identificar (en lugar de descartar) la fibrosis avanzada, a pesar del índice de probabilidad positivo insatisfactorio de estas pruebas. Las pautas también mencionan FibroScan® y elastografía por resonancia magnética. Sin embargo, no hay recomendaciones para un enfoque gradual. Las guías de la Sociedad Británica de Gastroenterología recomiendan el uso del score NFS o FIB-4 como primer paso en todos los pacientes diagnosticados con EHGNA. Los pacientes con un riesgo indeterminado deben someterse a pruebas en centros especializados, con puntuación ELF o una técnica de elastografía, según la disponibilidad local y la experiencia. Este es un enfoque práctico, que indica la necesidad de acción y mayor consideración sin ser demasiado prescriptivo.
NICE consideró que la prueba de fibrosis avanzada era coste-efectiva en EHGNA, aunque concluyó de manera controversial, que el uso de la puntuación ELF era el enfoque más rentable. Esta conclusión se debió probablemente al hecho de que la precisión diagnóstica de la puntuación ELF imputada en el modelo fue extrapolada de un estudio pediátrico de 112 pacientes que informaron de una sensibilidad del 100% y una especificidad del 98% para esta prueba. Tapper y colegas compararon la rentabilidad del score NFS, FibroScan®, una combinación de NFS y FibroScan®, y la biopsia de hígado, y encontraron que el NFS solo o en combinación con FibroScan® era la opción más rentable, según el escenario utilizado. De manera similar, nuestro análisis de costes indicó que un enfoque de dos niveles, con una combinación de una prueba simple no invasiva añadiendo ELF o FibroScan®, condujo a una tasa de referencia del 10% y ahorros sustanciales de costes en comparación con un solo nivel.
Parece creciente que se requieren pruebas no invasivas para la detección de fibrosis avanzada en pacientes con EHGNA y que debe extenderse a pacientes con riesgo de NASH, incluso cuando no se presenta un diagnóstico concluyente. Esta extensión para pacientes de alto riesgo tiene varios beneficios potenciales, puesto que las pruebas de diagnóstico para la esteatosis son subóptimas, aumentaría la aceptación de las pruebas al simplificar los algoritmos disponibles, aumentaría la conciencia de la enfermedad y cambiaría el enfoque de los médicos hacia un diagnóstico clínicamente significativo. Los pacientes deben volver a realizarse la prueba después de 3 a 5 años, para evaluar si ha habido una progresión de la enfermedad o los posibles falsos negativos del episodio diagnóstico inicial.
Manejo de la EHGNA en atención primaria
El enfoque principal del manejo en la atención primaria debe ser el tratamiento de las comorbilidades metabólicas para reducir el riesgo cardiovascular, que también puede prevenir el desarrollo futuro de EHGNA con fibrosis. De hecho, los médicos de atención primaria están mucho mejor equipados para enfrentar estos riesgos que los hepatólogos en la atención secundaria. Las intervenciones en el estilo de vida con dieta y ejercicio son el primer paso clave para todos estos pacientes. Una pérdida de peso del 10% fue, en un estudio, se asoció con la resolución de NASH en el 90% de los pacientes con EHGNA y la mejora de la fibrosis en el 45% de los pacientes. La cirugía bariátrica es una opción efectiva en pacientes seleccionados que cumplen criterios particulares de obesidad o comorbilidad. Además, el ejercicio regular reduce la grasa visceral y hepática, incluso en ausencia de pérdida de peso.
Con respecto a la farmacoterapia, algunos medicamentos podrían considerarse para el tratamiento de las comorbilidades metabólicas, en algunos casos, debido a un beneficio sugerido en la EHGNA. La mayoría de los resultados sobre este tema, a excepción de los estudios con pioglitazona, provienen de estudios observacionales o pilotos y deberán verificarse en ensayos controlados aleatorios con el poder estadístico adecuado. En un estudio nacional de casos y controles de Taiwán, la metformina se asoció con un riesgo reducido de carcinoma hepatocelular en pacientes con diabetes. La metformina se recomienda como tratamiento de primera línea para la diabetes tipo 2. La pioglitazona tuvo efectos positivos en la histología hepática y es una opción razonable para agregar al tratamiento en algunos pacientes con diabetes tipo 2 y EHGNA que no presentan contraindicaciones relevantes.
El tratamiento con liraglutida dio como resultado una pérdida de peso y una mejor histología en los pacientes con EHGNA, como se mostró en un ensayo controlado aleatorizado de prueba de concepto. Los bloqueadores de la angiotensina II podrían tener efectos antifibróticos y podrían ser el tratamiento de primera línea para pacientes con hipertensión arterial comórbida. El riesgo cardiovascular general debe calcularse para todos los pacientes con EHGNA (o con alto riesgo de EHGNA) mediante el uso de las herramientas adecuadas (como la puntuación QRISK2), y las estatinas deben iniciarse si es necesario. Existe una percepción infundada de un mayor riesgo de hepatotoxicidad causada por las estatinas en pacientes con concentraciones anormales de aminotransferasas entre los especialistas no hepatólogos, lo que hace que los pacientes no puedan recibir un medicamento esencial. Un análisis post-hoc de 437 pacientes con concentraciones moderadamente elevadas de aminotransferasas (probablemente debido a EHGNA) y que participaron en el estudio GREACE mostró que el tratamiento con estatinas era seguro y podría mejorar las concentraciones de aminotransferasas y reducir la morbilidad cardiovascular. Las concentraciones basales de aminotransferasas no tienen un mayor riesgo de hepatotoxicidad que las personas con concentraciones normales.
Conclusiones
- La creciente carga de la obesidad es un problema preocupante para la salud pública y se relaciona con la elevada prevalencia global de EHGNA de más del 25%.
- La atención primaria tiene un papel importante en la prevención del desarrollo y la progresión de EHGNA y en la detección de pacientes con riesgo de enfermedad crónica hepática, y con derivación a atención especializada según sea necesario.
- Casi todos estos pacientes permanecerán en atención primaria y, por lo tanto, es esencial centrarse en el manejo activo de los factores de riesgo cardiovascular.
- Existe una necesidad urgente de un protocolo integrado entre la atención primaria y la especializada, para el diagnóstico mediante pruebas de fibrosis avanzada y derivaciones posteriores.
- La ausencia de protocolos generalizados da como resultado estrategias de derivación particulares que pueden pasar por alto a una proporción importante de población en riesgo.
- El despliegue de hepatólogos comunitarios y enfermeras especializadas podría ayudar a educar a los médicos generales y aumentar la concienciación.
- Se requiere más investigación sobre la necesidad de la detección de EHGNA y también sobre la mejor manera de detectar la presencia de fibrosis avanzada.
Fuente: thelancet.com/gastrohep, Vol 3 July 2018.
Autores: Emmanuel A. Tsochatzis y Philip N. Newsome.
Artículo traducido y adaptado por ASSCAT
